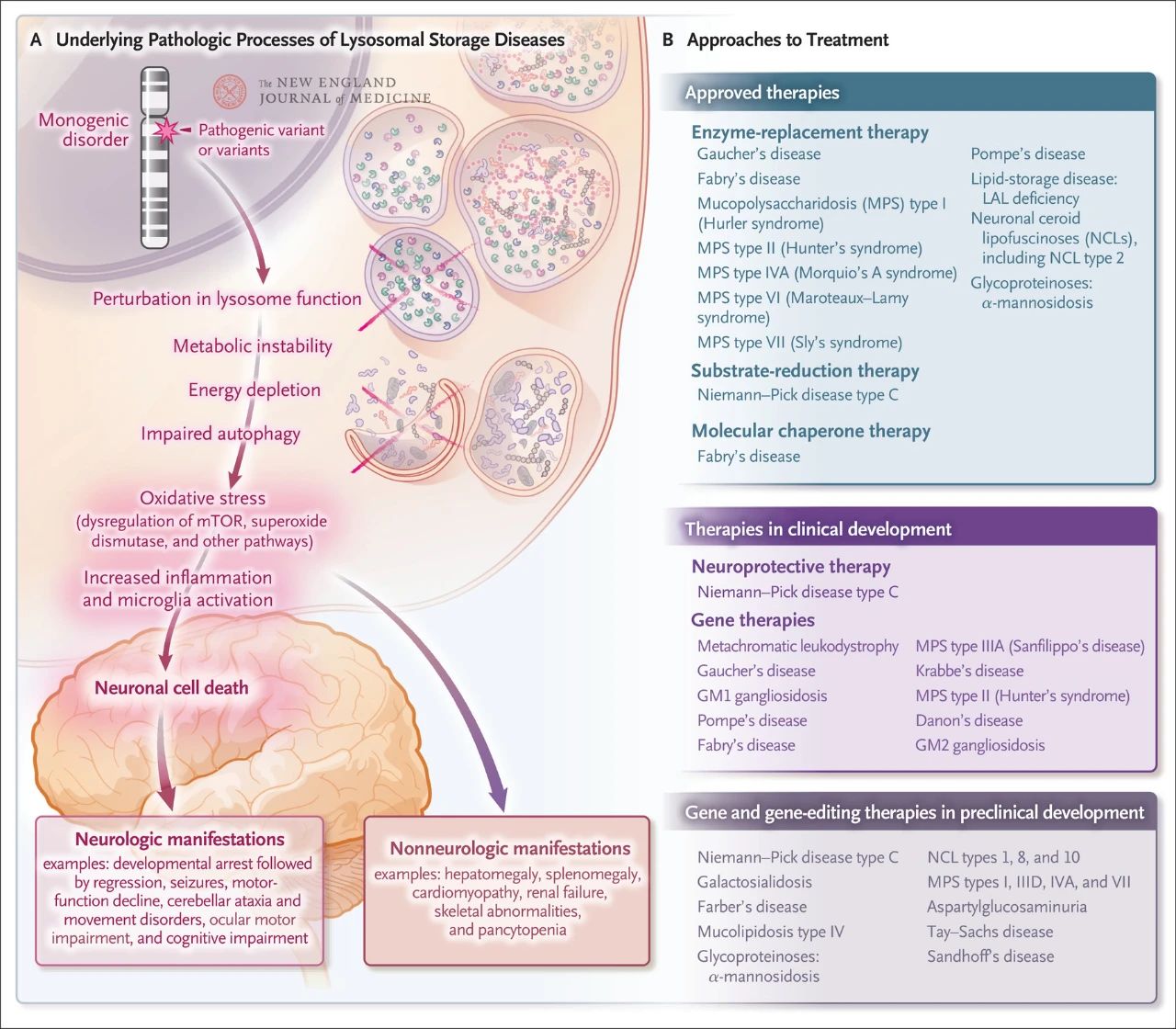
Även om det är relativt sällsynt är den totala incidensen av lysosomal lagring ungefär 1 av 5 000 levande födda. Dessutom påverkar 70 % av de nästan 70 kända lysosomala lagringssjukdomarna det centrala nervsystemet. Dessa enstaka gensjukdomar orsakar lysosomal dysfunktion, vilket resulterar i metabolisk instabilitet, dysreglering av däggdjursmålproteinet rapamycin (mTOR, som normalt hämmar inflammation), nedsatt autofagi och nervcellsdöd. Flera terapier som riktar sig mot de underliggande patologiska mekanismerna för lysosomal lagringssjukdom har godkänts eller är under utveckling, inklusive enzymersättningsterapi, substratreduktionsterapi, molekylär chaperonterapi, genterapi, genredigering och neurobeskyddande terapi.
Niemann-Picks sjukdom typ C är en lysosomal cellulär kolesteroltransportstörning orsakad av bialleliska mutationer i antingen NPC1 (95 %) eller NPC2 (5 %). Symtomen på typ C av Niemann-Picks sjukdom inkluderar snabb, dödlig neurologisk nedgång i spädbarnsåldern, medan de sena formerna med juvenil, juvenil och vuxen debut inkluderar splenomegali, supranukleär blickförlamning och cerebellär ataxi, dysartikulationsi och progressiv demens.
I detta nummer av tidskriften rapporterar Bremova-Ertl et al. resultaten av en dubbelblind, placebokontrollerad crossover-studie. Studien använde ett potentiellt neurobeskyddande medel, aminosyraanalogen N-acetyl-L-leucin (NALL), för att behandla Niemann-Picks sjukdom typ C. De rekryterade 60 symtomatiska ungdomar och vuxna patienter och resultaten visade signifikant förbättring av den totala poängen (primärt effektmått) på Ataxia Assessment and Rating Scale.
De kliniska prövningarna av N-acetyl-DL-leucin (Tanganil), en racemisk av NALL och n-acetyl-D-leucin, verkar till stor del vara erfarenhetsdrivna: verkningsmekanismen har inte klarlagts tydligt. N-acetyl-dl-leucin har godkänts för behandling av akut vertigo sedan 1950-talet; Djurmodeller tyder på att läkemedlet fungerar genom att återbalansera överpolariseringen och depolariseringen av mediala vestibulära neuroner. Därefter rapporterade Strupp et al. resultaten av en korttidsstudie där de observerade förbättringar av symtom hos 13 patienter med degenerativ cerebellär ataxi av olika etiologier, fynd som återuppväckte intresset för att undersöka läkemedlet igen.
Mekanismen genom vilken n-acetyl-DL-leucin förbättrar nervfunktionen är ännu inte klarlagd, men resultaten i två musmodeller, en av Niemann-Picks sjukdom typ C och den andra av GM2 gangliosidlagringsstörning variant O (Sandhoffs sjukdom), en annan neurodegenerativ lysosomal sjukdom, har fått uppmärksamheten att riktas mot NALL. Mer specifikt förbättrades överlevnaden hos Npc1-/- möss behandlade med n-acetyl-DL-leucin eller NALL (L-enantiomerer), medan överlevnaden hos möss behandlade med n-acetyl-D-leucin (D-enantiomerer) inte gjorde det, vilket tyder på att NALL är den aktiva formen av läkemedlet. I en liknande studie av GM2 gangliosidlagringsstörning variant O (Hexb-/-) resulterade n-acetyl-DL-leucin i en blygsam men signifikant förlängning av livslängden hos möss.
För att utforska verkningsmekanismen för n-acetyl-DL-leucin undersökte forskarna leucins metaboliska väg genom att mäta metaboliter i lillhjärnans vävnader hos de muterade djuren. I en variant O-modell av GM2-gangliosidlagringsstörning normaliserar n-acetyl-DL-leucin glukos- och glutamatmetabolismen, ökar autofagi och ökar nivåerna av superoxiddismutas (en aktiv syrefångare). I C-modellen av Niemann-Picks sjukdom observerades förändringar i glukos- och antioxidantmetabolism och förbättringar i mitokondriell energimetabolism. Även om L-leucin är en potent mTOR-aktivator, skedde ingen förändring i nivån eller fosforyleringen av mTOR efter behandling med n-acetyl-DL-leucin eller dess enantiomerer i någon av musmodellerna.
Den neurobeskyddande effekten av NALL har observerats i en musmodell av hjärnskada inducerad av kortikal impingement. Dessa effekter inkluderar sänkning av neuroinflammatoriska markörer, minskad kortikal celldöd och förbättrat autofagiflöde. Efter NALL-behandling återställdes de motoriska och kognitiva funktionerna hos de skadade mössen och lesionsstorleken minskades.
Det inflammatoriska svaret i centrala nervsystemet är kännetecknande för de flesta neurodegenerativa lysosomala lagringssjukdomar. Om neuroinflammation kan minskas med NALL-behandling, kan de kliniska symtomen på många, om inte alla, neurodegenerativa lysosomala lagringssjukdomar förbättras. Som denna studie visar förväntas NALL också ha synergier med andra behandlingar för lysosomala lagringssjukdomar.
Många lysosomala lagringsstörningar är också associerade med cerebellär ataxi. Enligt en internationell studie med barn och vuxna med GM2-gangliosidlagringsstörningar (Tay-Sachs sjukdom och Sandhoffs sjukdom) minskade ataxi och finmotorik förbättrades efter NALL-behandling. Emellertid visade en stor, multicenter, dubbelblind, randomiserad, placebokontrollerad studie att n-acetyl-DL-leucin inte var kliniskt effektivt hos patienter med blandad (ärftlig, icke-ärftlig och oförklarlig) cerebellär ataxi. Detta fynd tyder på att effekt endast kan observeras i studier med patienter med ärftlig cerebellär ataxi och de associerade verkningsmekanismerna analyseras. Eftersom NALL minskar neuroinflammation, vilket kan leda till traumatisk hjärnskada, kan studier av NALL för behandling av traumatisk hjärnskada övervägas.
Publiceringstid: 2 mars 2024