Alzheimers sjukdom, det vanligaste fallet bland äldre, har plågat de flesta människor.
En av utmaningarna vid behandling av Alzheimers sjukdom är att tillförseln av terapeutiska läkemedel till hjärnvävnaden begränsas av blod-hjärnbarriären. Studien fann att MR-ledd lågintensiv fokuserad ultraljud reversibelt kan öppna blod-hjärnbarriären hos patienter med Alzheimers sjukdom eller andra neurologiska sjukdomar, inklusive Parkinsons sjukdom, hjärntumörer och amyotrofisk lateralskleros.
En nyligen genomförd liten proof-of-concept-studie vid Rockefeller Institute for Neuroscience vid West Virginia University visade att patienter med Alzheimers sjukdom som fick aducanumab-infusion i kombination med fokuserat ultraljud tillfälligt öppnade blod-hjärnbarriären signifikant minskade hjärnans amyloid beta (Aβ)-belastning på studiesidan. Forskningen skulle kunna öppna nya dörrar för behandlingar för hjärnsjukdomar.
Blod-hjärnbarriären skyddar hjärnan från skadliga ämnen samtidigt som den tillåter viktiga näringsämnen att passera. Men blod-hjärnbarriären förhindrar också leverans av terapeutiska läkemedel till hjärnan, en utmaning som är särskilt akut vid behandling av Alzheimers sjukdom. I takt med att världen åldras ökar antalet personer med Alzheimers sjukdom år för år, och behandlingsalternativen är begränsade, vilket lägger en stor belastning på sjukvården. Aducanumab är en amyloid beta (Aβ)-bindande monoklonal antikropp som har godkänts av US Food and Drug Administration (FDA) för behandling av Alzheimers sjukdom, men dess penetration av blod-hjärnbarriären är begränsad.
Fokuserad ultraljud producerar mekaniska vågor som inducerar oscillationer mellan kompression och utspädning. När bubblorna injiceras i blodet och exponeras för ultraljudsfältet komprimeras och expanderar de mer än den omgivande vävnaden och blodet. Dessa oscillationer skapar mekanisk stress på blodkärlsväggen, vilket gör att de täta kopplingarna mellan endotelcellerna töjs ut och öppnas (Figur nedan). Som ett resultat äventyras blod-hjärnbarriärens integritet, vilket gör att molekyler kan diffundera in i hjärnan. Blod-hjärnbarriären läker av sig själv på cirka sex timmar.
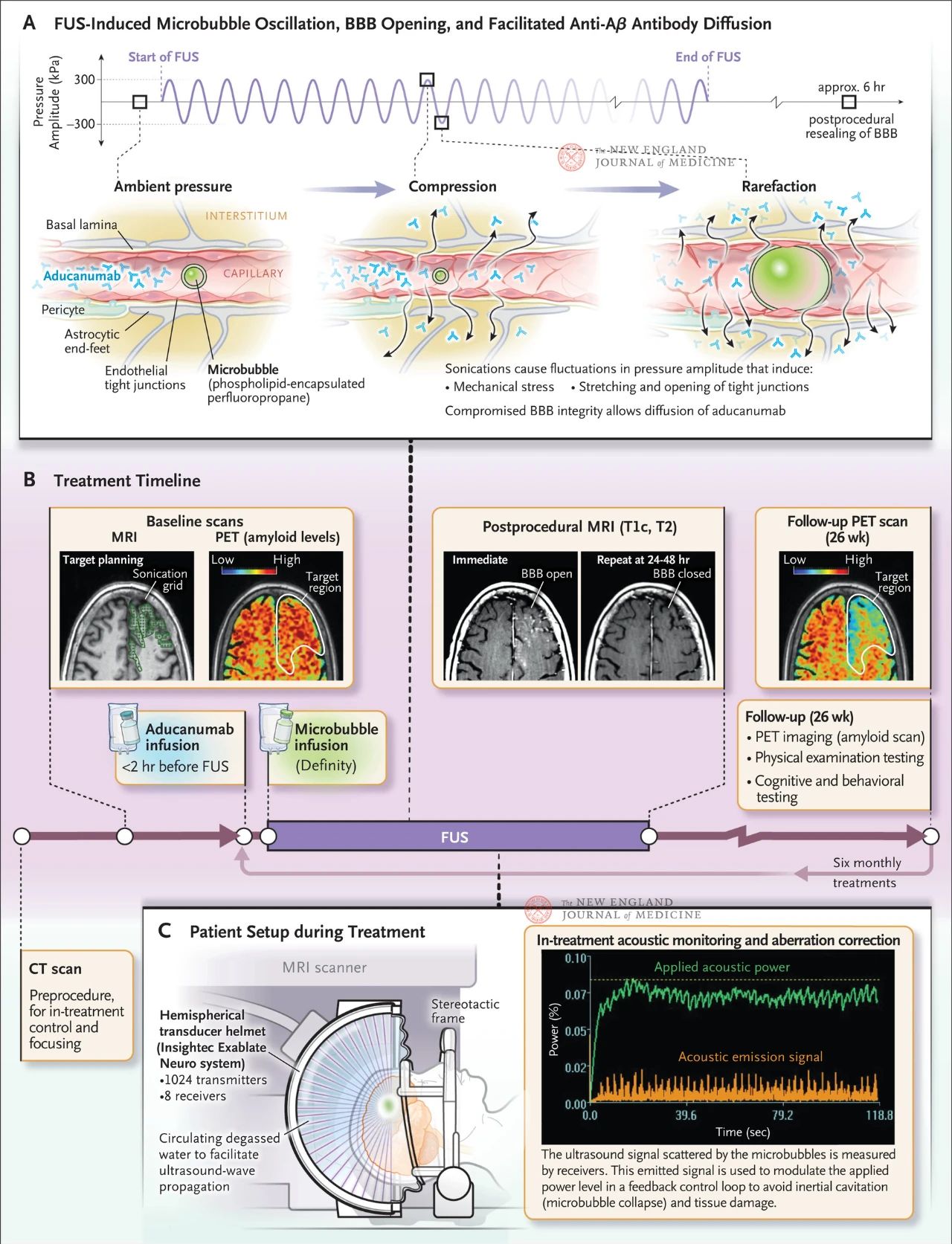
Figuren visar effekten av riktad ultraljud på kapillärväggar när mikrometerstora bubblor finns i blodkärl. På grund av gasens höga kompressibilitet drar sig bubblorna samman och expanderar mer än den omgivande vävnaden, vilket orsakar mekanisk stress på endotelcellerna. Denna process orsakar att täta förbindningar öppnas och kan också orsaka att astrocytändar faller av blodkärlsväggen, vilket äventyrar blod-hjärnbarriärens integritet och främjar antikroppsdiffusion. Dessutom förstärkte endotelceller som exponerats för fokuserat ultraljud sin aktiva vakuolära transportaktivitet och undertryckte effluxpumpfunktionen, vilket minskade hjärnans clearance av antikroppar. Figur B visar behandlingsschemat, vilket inkluderar datortomografi (CT) och magnetisk resonanstomografi (MRT) för att utveckla ultraljudsbehandlingsplanen, 18F-flubitaban positronemissionstomografi (PET) vid baslinjen, antikroppsinfusion före fokuserad ultraljudsbehandling och mikrovesikulär infusion under behandlingen, samt akustisk övervakning av de mikrovesikulära spridningsultraljudssignalerna som används för att kontrollera behandlingen. Bilderna som erhölls efter fokuserad ultraljudsbehandling inkluderade T1-vägd kontrastförstärkt MRI, som visade att blod-hjärnbarriären var öppen i det ultraljudsbehandlade området. Bilder av samma område efter 24 till 48 timmars fokuserad ultraljudsbehandling visade fullständig läkning av blod-hjärnbarriären. En PET-skanning med 18F-flubitaban under uppföljning hos en av patienterna 26 veckor senare visade minskade Aβ-nivåer i hjärnan efter behandling. Figur C visar den MRI-guidade fokuserade ultraljudsuppsättningen under behandlingen. Den halvsfäriska givarhjälmen innehåller mer än 1 000 ultraljudskällor som konvergerar till en enda fokuspunkt i hjärnan med hjälp av realtidsvägledning från MRI.
År 2001 visades det för första gången i djurstudier att fokuserat ultraljud inducerar öppningen av blod-hjärnbarriären, och efterföljande prekliniska studier har visat att fokuserat ultraljud kan förbättra läkemedelsleverans och effekt. Sedan dess har man funnit att fokuserat ultraljud säkert kan öppna blod-hjärnbarriären hos patienter med Alzheimers sjukdom som inte får medicinering, och kan även leverera antikroppar mot hjärnmetastaser i bröstcancer.
Leveransprocess för mikrobubblor
Mikrobubblor är ett ultraljudskontrastmedel som vanligtvis används för att observera blodflöde och blodkärl vid ultraljudsdiagnostik. Under ultraljudsbehandling injicerades en fosfolipidbelagd, pyrogenfri bubbelsuspension av oktafluoropropan intravenöst (Figur 1B). Mikrobubblor är mycket polydispersa, med diametrar från mindre än 1 μm till mer än 10 μm. Oktafluoropropan är en stabil gas som inte metaboliseras och kan utsöndras genom lungorna. Lipidskalet som omsluter och stabiliserar bubblorna består av tre naturliga humana lipider som metaboliseras på ett liknande sätt som endogena fosfolipider.
Generering av fokuserad ultraljud
Fokuserat ultraljud genereras av en halvklotformad givarehjälm som omger patientens huvud (Figur 1C). Hjälmen är utrustad med 1024 oberoende styrda ultraljudskällor, som är naturligt fokuserade i mitten av halvklotet. Dessa ultraljudskällor drivs av sinusformade radiofrekvensspänningar och avger ultraljudsvågor som styrs av magnetisk resonanstomografi. Patienten bär en hjälm och avgasat vatten cirkulerar runt huvudet för att underlätta ultraljudsöverföring. Ultraljudet färdas genom huden och skallen till hjärnmålet.
Förändringar i skallens tjocklek och densitet kommer att påverka ultraljudsutbredningen, vilket resulterar i en något annorlunda tid för ultraljudet att nå lesionen. Denna distorsion kan korrigeras genom att skaffa högupplösta datortomografidata för att få information om skallens form, tjocklek och densitet. En datorsimuleringsmodell kan beräkna den kompenserade fasförskjutningen för varje drivsignal för att återställa det skarpa fokuset. Genom att kontrollera RF-signalens fas kan ultraljudet fokuseras elektroniskt och positioneras för att täcka stora mängder vävnad utan att ultraljudskälluppsättningen flyttas. Målvävnadens plats bestäms genom magnetisk resonanstomografi av huvudet medan man bär hjälm. Målvolymen fylls med ett tredimensionellt rutnät av ultraljudsförankringspunkter, som avger ultraljudsvågor vid varje förankringspunkt i 5–10 ms, upprepade var tredje sekund. Ultraljudseffekten ökas gradvis tills den önskade bubbelspridningssignalen detekteras och hålls sedan i 120 sekunder. Denna process upprepas på andra nät tills målvolymen är helt täckt.
För att öppna blod-hjärnbarriären krävs att ljudvågornas amplitud överstiger ett visst tröskelvärde. Utöver detta ökar barriärens permeabilitet med ökande tryckamplitud tills vävnadsskada uppstår, vilket manifesteras som erytrocyt-exosmos, blödning, apoptos och nekros, vilka alla ofta är förknippade med bubbelkollaps (kallad tröghetskavitation). Tröskelvärdet beror på mikrobubblornas storlek och skalmaterialet. Genom att detektera och tolka ultraljudssignalerna som sprids av mikrobubblorna kan exponeringen hållas inom ett säkert intervall.
Efter ultraljudsbehandling användes T1-viktad MR med kontrastmedel för att avgöra om blod-hjärnbarriären var öppen vid målplatsen, och T2-viktade bilder användes för att bekräfta om extravasation eller blödning inträffade. Dessa observationer ger vägledning för att justera andra behandlingar, om det behövs.
Utvärdering och utsikter till terapeutisk effekt
Forskarna kvantifierade effekten av behandlingen på hjärnans Aβ-belastning genom att jämföra 18F-flubitaban positronemissionstomografi före och efter behandling för att bedöma skillnaden i Aβ-volym mellan det behandlade området och ett liknande område på motsatt sida. Tidigare forskning av samma team har visat att enbart fokusering på ultraljud kan minska Aβ-nivåerna något. Den minskning som observerades i denna studie var ännu större än i tidigare studier.
I framtiden kommer det att vara avgörande att utöka behandlingen till båda sidor av hjärnan för att utvärdera dess effektivitet när det gäller att fördröja sjukdomsprogression. Dessutom behövs mer forskning för att fastställa långsiktig säkerhet och effekt, och kostnadseffektiva terapeutiska apparater som inte är beroende av online-MR-vägledning måste utvecklas för bredare tillgänglighet. Resultaten har dock väckt optimism om att behandlingen och läkemedlen som eliminerar Aβ så småningom kan bromsa Alzheimers progression.
Publiceringstid: 6 januari 2024